Temas
La Materia y Sus Estados de Separación
La materia es todo lo que tiene masa y ocupa un espacio,
estando ya sea en estado líquido, solido, gaseoso o plasma, la materia se puede
dividir en dos, en sustancias puras donde encontramos elementos y compuestos o
en mezclas donde encontramos homogénea y heterogénea. La materia tiene
propiedades física, donde no se altera la estructura interna y las propiedades químicas, donde se altera la
estructura interna. (quimico, 2016)
NOMBRE DE SEPARACION
|
USO
|
GRAFICA
|
Decantación
|
Se usa para separar líquidos inmiscibles.
|
|
Filtración
|
Se usa para separar un sólido
de un líquido.
|
|
Evaporación
|
Se usa para separar un sólido disuelto en el líquido.
|
|
Destilación
|
Se usa para separar mezclas de líquidos miscibles, así como solidos
disueltos en un líquido.
|
|
Centrifugación
|
Se usa para separar un sólido de tamaño fino suspendido en un líquido
de diferente densidad mediante una fuerza centrifugada.
|
|
Cromatografía
|
Se usa para separar dos mezclas liquidas.
|
|
Magnetismo
|
Se usa para separar sólidos con magnesio
|
Conversión de Unidades
La conversión de unidades es la transformación de un valor numérico de una magnitud física en otro valor numérico equivalente, expresado en otra unidad de medida por medio de factores de conversión, por este método se logra obtener un resultado más eficaz que por medio de otros medios.
Estructura atómica
El Átomo
El átomo es la cantidad más pequeña de un elemento, esta conformado por tres partes las cuales son los protones con carga parcialmente positiva, los electrones con carga parcialmente negativa y los neutrones con carga neutra. Los átomos pueden ser isótopos o iones. Los isotopos son átomos con el mismo número atómico (número de protones en el núcleo), pero diferente número másico (suma del número de neutrones y el de protones de un núcleo). Los iones son átomos que se comparten electrones para cumplir la ley del octeto, donde cuando se gana un electrón queda en carga negativa y se les llama anión, y cuando se pierde un electrón queda en carga positiva y se les llama catión.
Las partículas subatómicas se constituyen por el símbolo del elemento, el número atómico el cual es el número de electrones en las orbitas o el número de protones en el núcleo, y el número de masa o másico el cual es la suma del número de protones y neutrones.
Números
Los números cuánticos son parámetros que
describen el estado energético de un electrón y las características de un
orbital. Los numero cuánticos son:
(Química, Química Inorgánica, 2012)
Tabla
La tabla periódica es una herramienta que nos ayuda a clasificar y organizar los elementos químicos de acuerdo a sus propias características y propiedades.
Las columnas verticales de la tabla periódica se les conocen como grupos y están numerados por números romanos, ya que tienen la misma capa de valencia atómica.
- Grupo 1 (I A): los metales alcalinos
- Grupo 2 (II A): los metales alcalinotérreos
- Grupo 3 (III B): Familia del Escandio
- Grupo 4 (IV B): Familia del Titanio
- Grupo 5 (V B): Familia del Vanadio
- Grupo 6 (VI B): Familia del Cromo
- Grupo 7 (VII B): Familia del Manganeso
- Grupo 8 (VIII B): Familia del Hierro
- Grupo 9 (IX B): Familia del Cobalto
- Grupo 10 (X B): Familia del Níquel
- Grupo 11 (I B): Familia del Cobre
- Grupo 12 (II B): Familia del Zinc
- Grupo 13 (III A): los térreos
- Grupo 14 (IV A): los carbonoideos
- Grupo 15 (V A): los nitrogenoideos
- Grupo 16 (VI A): los calcógenos o anfígenos
- Grupo 17 (VII A): los halógenos
- Grupo 18 (VIII A): los gases nobles
Las filas horizontales de la tabla periódica son llamadas períodos,
se encuentran 7 filas en la tabla
periódica. Los elementos que componen una misma fila tienen propiedades
diferentes pero masas similares: todos los elementos de un período tienen el
mismo número de orbitales.
Los bloques o regiones se denominan según la letra que hace referencia al orbital más externo: s, p, d y f. Estos se pueden clasificar en dos divisiones los representativos ( S o P) y los de transición (D o F).
El radio atómico de un elemento es la mitad de la distancia entre
los centros de dos átomos vecinos. Aumenta al descender en los grupos de la tabla periódica y
disminuye al avanzar a lo largo un periodo. Se indican a menudo
en angstroms A
10-10m), nanómetros (nm, 10-9 m) picometro (pm,
10-12 m). (Quimica P. , 2015)
La
electronegatividad es la tendencia de los átomos de atraer los electrones de
otros átomos cuando se unen con ellos. Aumenta al ascender en los grupos y de izquierda a derecha en los periodos,
siendo flúor el elemento más electronegativo y el Francio el menos
electronegativo. (Electronegatividad, 2016)
Enlace Químico.
Estructura de Lewis: referente a la organización de electrones en un átomo.
Existen tres tipos de enlace: iónico, covalente y metálico.
Enlaces iónicos
Se caracterizan por:
- Ser sólidos cristalinos.
- Tener altos puntos de fusión y ebullición.
- Ser buenos conductores de electricidad.
- Solubles en agua.
- Tienen una electronegatividad mayor a 1.7.
Pueden ser simples, dobles o triples.
Se clasifican en polar, apolar y dativo.
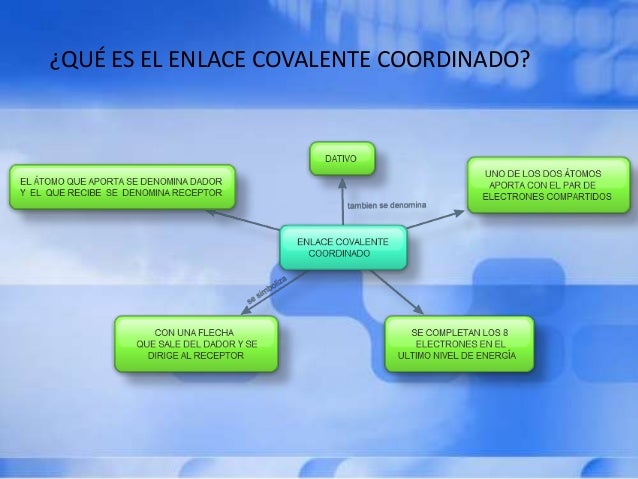
El enlace covalente dativo o coordinado se da en un contexto extremo ya que no cumple la principal regla entre los covalentes que es compartir porque solo uno da y otro recibe.
Enlace Metálico
Funciones químicas inorgánicas y Nomenclatura.
Las funciones químicas son grupos de compuestos que presentan algunas propiedades químicas semejantes. Se encuentran cinco principalmente.
La nomenclatura sirve para nombrar compuestos referentes a las funciones quimicas.
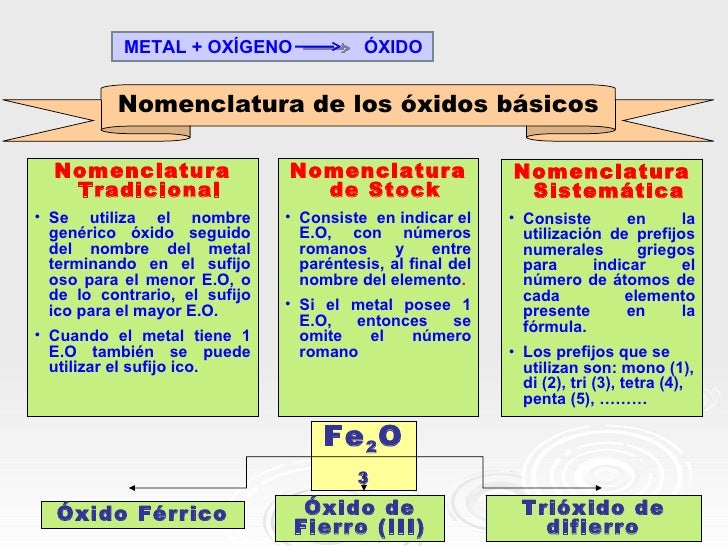
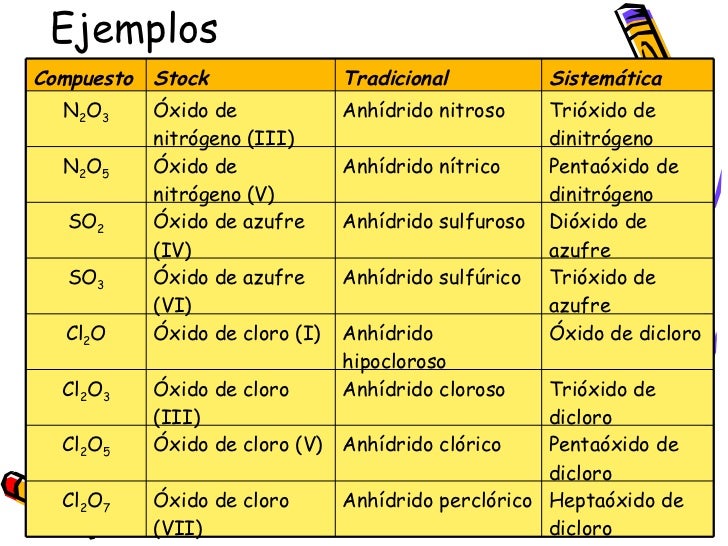
Óxido.
- Mayoría de elementos con oxígeno.
- Son compuestos binarios.
Ácidos.
Se caracterizan por:
- Comenzar por H.
- Enlazarse con no metales.
Existen dos clases:
Óxacido: Se define como la unión entre un hidrógeno, un no metal y oxigeno.
Hidracido: Combinación entre hidrógeno y no metal.
Sales.
Se caracterizan por contener un metal y un no metal.
Se clasifican en:
- Oxisales: M+NM+O
- Halogenas: binarias.
Hidruros.
Se caracterizan porque el estado de oxidación del H es -1
En resumen:
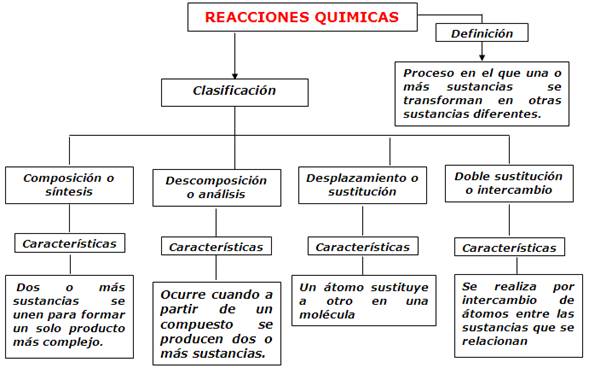
Tipos de reacciones.
Balanceo de ecuaciones por tanteo.
Sirve para cumplir la ley de la conservación de la materia.
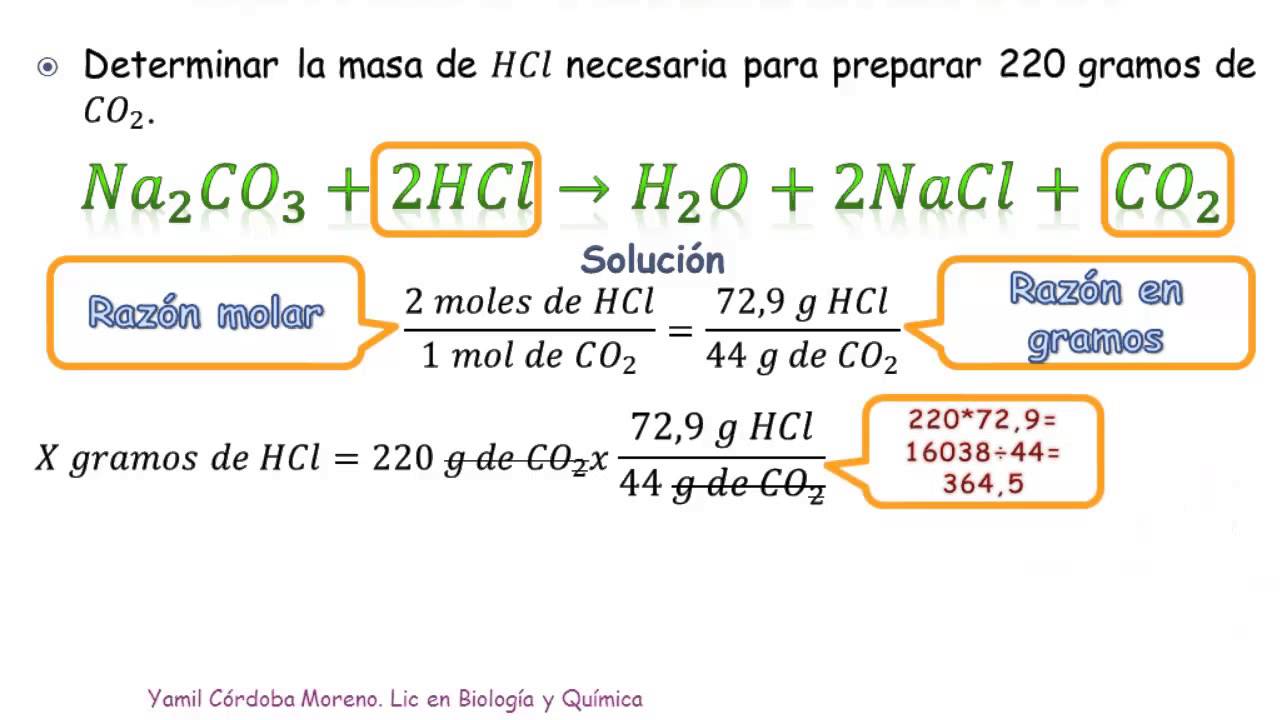
Estequiometría.
Es el cálculo de las relaciones cuantitativas entre los reactivos y los productos en el transcurso de una reacción química.
Soluciones.
También son llamadas disoluciones y son mezclas homogéneas, compuestas de:
Soluto: lo que se disuelve y suele estar en menor cantidad.
Solvente: Medio dispersor y esta en mayor cantidad.
La solucion es la suma del soluto y el solvente.
Tipos de soluciones
- In-saturada o diluida: - soluto, + solvente.
- Sobre-saturada: + soluto, - solvente.
- Saturada: cantidad ideal entre el soluto y solvente.
Solubilidad
Se define como la capacidad máxima de una sustancia de disolverse en otra.
Factores que afectan la solubilidad:
- Temperatura
- Presión
- Agitación
- Superficie de contacto
- Naturaleza de las sustancias
Unidades de concentración:


























Comentarios
Publicar un comentario